
Postprandiell lipid och glukosmetabolism och dess behandlingsmöjligheter
Av Mette Axelsen, Göteborg..
Denna artikel är baserad på avhandlingen Nocturnal and postprandial metabolism in diabetes mellitus, som försvarades den 8 april i år.
Postprandiell lipidintolerans
Fyrtio (1) till 50 procent (2) av nydebuterade Typ 2 diabetiker har redan etablerat hjärt-kärlsjukdom vid tiden för diagnos. Sannolikt bär man på riskfaktorer under många år innan diabetes bryter ut. Därför är det viktigt att riskfaktorer identifieras så att behandling kan erbjudas tidigt till högrisk-individer. Dock har alla tillgängliga data visat att t ex fastelipiderna är normala hos dessa personer (3-9).
Att mäta triglyceriderna efter måltid, istället för i fasta, innebär att man kan identifiera personer med hjärt-kärlsjukdom (10-12). Det har också visats att förhöjda postprandiella koncentrationer av chylomikron restpartiklar på samma sätt som LDL kan ge upphov till hjärt-kärlsjukdom. Postprandiell lipemi är därför ansedd som en riskfaktor för hjärt-kärlsjukdom.
Vi studerade postprandiella triglycerider hos en grupp insulinresistenta män med hög ärftlig risk för att senare i livet drabbas av Typ 2 diabetes (9). Den genomsnittliga åldern var 34 år. Deltagarna fick på fastande mage äta en standardiserad frukost med varm choklad och ostfralla.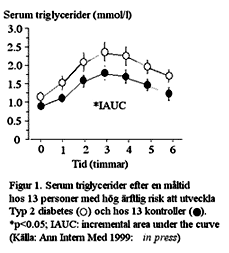
Under sex timmar efter måltiden uppmättes nedbrytningen av försökspersonernas blodfetter. Jämfört med en välmatchad kontrollgrupp utan känd diabetesärftlighet hade högrisk-gruppen 50 procent högre postprandiell triglyceridrespons efter måltiden (Fig. 1).
Kan hjärt-kärlsjukdom förebyggas?
Vår upptäckt att personer med insulinresistens och hög diabetesärftlighet har lipidintolerns (9) kan betyda att det går att förebygga hjärt-kärlsjukdom hos Typ 2 diabetiker genom tidiga insatser. Deltagarna hade normala fastelipider, normal glukostolerans, normal midje/höft-kvot, normal vikt och var icke-rökare.
Lipidintoleransen uppträder alltså i allt väsentligt i avsaknad av andra kliniska riskfaktorer för hjärt-kärlsjukdom. Ett särskilt diagnostiskt lipidtoleranstest skulle krävas för att fånga dessa prediabetiska personer med hög risk att utveckla kranskärlssjukdomar. Fortfarande saknas dock ett diagnostiskt test som kan mäta halten postprandiella triglycerider efter måltid.
Det tar lång tid för kroppen att eliminera fettet i en måltid, vilket ställer särskilda krav på ett sådant test om det skall ge ett snabbt utslag på lipidintoleransen.
Mekanismer
Den underliggande mekanismen till lipidintoleransen hos prediabetiker är ännu inte kartlagd. Vi har tidigare visat att lipidintolerans finns hos rökare (13-15), vilka också karakteriseras av insulinresistens (16). Det är också känt att Typ 2 diabetiker har postprandiell hypertriglyceridemi, ibland till trots för normala fastetriglycerider. Professor Taskinens grupp i Helsingfors har tidigare påvisat att postprandiell lipidintolernas vid Typ 2 diabetes beror på en försämrad undertryckning av VLDL1-frisättningen från levern som svar på insulin (17).
Vår hypotes är att den postprandiella lipidintoleransen är ett kardinalfynd tidigt i diabetesutvecklingen och att mekanismen hos friska högrisk-individer är densamma som hos Typ 2 diabetiker, d.v.s. kopplad till insulinresistens. En ökad VLDL-frisättning leder i sin tur till ökad retention av chylomikron restpartiklar (15, 18) och små, täta LDL-partiklar med ökad affinitet till proteoglykaner och därmed ökad atherosklerosbenägenhet (19).
Samtliga dessa faktorer, och deras behandling, är därför viktiga att studera hos personer med predisposition för Typ 2 diabetes. Det är även viktigt för framtida forskning att undersöka om de nya fynden även gäller kvinnor i högriskzonen.
Så här kan nattliga hypoglykemier förebyggas
Ett helt annat problem, som omfattar många Typ 1 diabetiker, är låga blodsockervärden nattetid. Frekvensen av nattliga hypoglykemier är ca 5 ggr vanligare med dagens intensivbehandling med insulin (20-22). De kan t ex yttra sig i form av orolig sömn, svettningar och mardrömmar.
Nattliga hypoglykemier är potentiellt farliga av flera anledningar:
1) under sömnen är patientens förmåga att reagera på autonoma varningssignaler nedsatt (23). En initialt mild hypoglykemi kan därmed lättare progrediera till en svår hypoglykemi, detta vid en tidpunkt när hjälpen från utomstående kan vara begränsad;
2) en ökad insöndring av motregulatoriska hormoner till följd av nattlig hypoglykemi kan leda till hyperglykemi i upp till 8 timmar (24);
3) upprepade nattliga hypoglykemier kan inducera hypoglycemia unawareness, dvs sänkt förmåga att igenkänna en analkande hypoglykemi.
Detta i sin tur ger ökad risk för allvarliga hypoglykemier vid vilken tidpunkt som helst på dagen (25, 26).
Vi studerade effekten av att inta oupphettad majsstärkelse (maizenamjöl), en källa till långsamma kolhydrater, hos 12 Typ 1 diabetiker (27). Majsstärkelsen löstes i kallt vatten och smaksattes. Jämfört med stärkelsefri placebo var antalet låga nattliga blodsockervärden 70procent färre hos de patienter som fick dricka oupphettad majsstärkelse före sänggåendet (Fig. 2). Dosen som användes var 0.3g stärkelsepulver/kg kroppsvikt.
I båda perioderna vidtog patienterna alla kända traditionella åtgärder för undvikandet av nattlig hypoglykemi, dvs. mätning av blodsockernivån före sängdags, intag av mat om blodsockernivån var under 6-8 mmol/l, och anpassning av nattinsulindosen i förhållande till graden av fysisk aktivitet under dagen. Trots detta kunde den enkla majsstärkelsesupplementeringen ytterligare minska frekvensen av nattliga hypoglykemier med mer än hälften jämfört med det som idag är klinisk praxis.
Generellt är hypoglykemier vanligast runt 3-tiden på natten med normalt förfarande med NPH-insulin vid 11-tiden. Anledningen är att insulinkänsligheten är hög vid 3-tiden på natten (28, 29). Samtidigt har man en maximal insulineffekt vid samma tid, vilket därmed inte är i fas med insulinbehovet. Därefter avklingar insulineffekten från kl. 5 på morgonen och framåt, dvs vid en tid då man börjar bli insulinresistent och skulle behöva mer insulin.
Detta leder till ett klassiskt problem vid Typ 1 diabetes: Problemet att avväga insulindosen på ett sådant sätt att man undviker både hypoglykemier på natten och fastehyperglykemi på morgonen. Vår studie visade att majsstärkelsen i detta avseende kan balansera den nattliga insulineffekten och medge god blodsockerkontroll både natt och morgon (27). När den nattliga postprandiella glukosprofilen efter oupphettad majsstärkelse jämfördes med profilen efter en vanlig smörgås måltid, visades att smörgåsmåltid gav en kraftig blodsockertopp redan efter två timmar (27).
Detta är en tidpunkt när man egentligen inte behöver en blodsockertopp. Majsstärkelsen gav istället en lägre och betydligt mer utdragen blodsockerhöjande effekt, med sin maximala effekt efter ca. 4 timmar. Den sammanfaller därmed väl med den tidpunkt då glukosbehovet är som störst.
Livsmedel med lågt glykemisk index efterlystes
Typ 1 diabetikerna sade sig vara positiva till majsstärkelsen. De upplevde att detta var något de kunde tänka sig att fortsätta ta. Dock efterlyste de en rejäl produktutveckling. Majsstärkelsen smakar visserligen ingenting men den har en kritaktig konsistens som kan upplevas som obehaglig. Ett stort problem är att det är brist på stärkelserika livsmedel med s.k. långsamma kolhydrater. I en av studierna visades att oupphettad majsstärkelse hade ett glykemiskt index runt 50 (30). Detta är ett väldigt lågt värde, och de enda idag kända livsmedlena med så lågt glykemiskt index är bönor, linser och pumpernickelbröd (31) .
Majsstärkelsen får heller inte behandlas - kokas, etc - om man vill kvar den långsamma effekten. Upphettad majsstärkelse, som i bröd, välling o dyl, har inte alls samma effekt som oupphettad. Tvärtom. Kokt majsstärkelse förvandlas till snabb stärkelse och har samma - i sammanhanget negativa - verkan som t ex smörgås. Framtagandet av smakliga alternativ till majsstärkelsen är därför angeläget.
Nattlig kostterapi för Typ 2 diabetiker?
Ytterligare ett användingsområde då långsamma kolhydrater skulle kunna nyttjas, är inom den nattliga metabolismen hos Typ 2 diabetiker, och då i synnerhet genom att undertrycka de förhöjda nattliga nivåerna av fria fettsyror (FFA). Fria fettsyror försämrar blodsockerkontrollen, dels genom att öka leverns glukosproduktion (32, 33), dels genom minskat glukosupptag i muskel (34, 35), och även genom att hämma insulinsekretionen (36-39) och inducera programmerad cell-död i betacellerna (40). För att studera effekten av nattlig FFA undertryckning på glukos och lipidmetabolism påföljande morgonen fick Typ 2 diabetiker dricka oupphettad majsstärkelse före sänggåendet.
Undersökningarna visade att Typ 2 diabetikerna fick en 30 procentig undertryckning av plasma-FFA mellan kl 02 och 07 (41). Detta var i sin tur associerat med bättre fasteblodsockervärde och lägre blodsockertopp efter frukost (42).
En bidragande orsak kan ha varit den förbättrade insulinsekretionen postprandiellt. Dock förbättrades inte de postprandiella triglyceriderna. Erfarenheterna med majsstärkelsen hos Typ 2 diabetiker visade vidare att det är vanskligt att hos denna patientgrupp moderera mängderna stärkelse så att en positiv effekt på morgonens blodsockerkontroll erhålls utan att de nattliga blodsockervärdena påtagligt stiger. Dessutom verkade den mest lovande effekten föreligga för nydebuterade och insulinresistena patienter med välbevarad insulinsekretion.
I det fortsatta arbetet är det därför angeläget att realistiska långsamma livsmedelsprodukter testas hos personer med nedsatt glukostolernas och mild diabetes. Kommande studier Under det kommande året kommer jag gästa Professor David Jenkins vid Dept. of Nutritional Sciences, University of Toronto, Canada. Deras forskningprogram omfattar bl a effekten av hela koster, antioxidanter och vegetabiliska proteiner på glykemisk och lipidemisk kontroll hos personer med diabetes. Jag kommer under denna period bl a att beredas möjlighet att arbeta med en produktkedja med hel- och halvfabrikat med lågt glykemisk index (Too Good To Be True(tm)).
Frågeställningarna inkluderar:
Jag kommer även att i det fortsatta arbetet studera följande frågeställningar:
- Kommer en kost bestående av speciella produkter med lågt glykemiskt
index att resultera i mätbara förbättringar i blodsockerkontroll (HbA1c) hos Typ 2
diabetiker under kontrollerade omständigheter?
- Hur accepteras kosten och hur är långtidseffekten på blodsockerkontrollen
hos fritt levande individer?
Denna artikeln vill jag tillägna Stiftelsen för Vetenskapligt Arbete inom Diabetologi
- Vad är den underliggande mekanismen till den postprandiella lipidintolerans hos friska
personer med hög risk för Typ 2 diabetes
- Vad är effekten av olika typer av intervention på postprandiell lipidmetabolism
samt på LDL-proteoglykanaffinitet.
som tack för deras post-doc stipendium.
Fullständiga referenslistan kan fås genom
DiabetoFax tfn 08 34 79 55
dokument 93052.
Mette Axelsen
Lundberglab för diabetesforskning
SU/Sahlgrenska
413 45 Göteborg
E-post: mette.axelsen@medicine.gu.se
Referenser
1. Uusitupa M, Siitonen O, Aro A, Pyörälä K. Prevalence of coronary heart disease, left ventricular failure and hypertension in middle-aged, newly diagnosed Type 2 (non insulin-dependent) diabetic subjects. Diabetologia 1985;28:22-27.
9. Axelsen M, Smith U, Eriksson J, Taskinen M-R, Jansson P-A. Postprandial hypertriglyceridemia and insulin resistance in normoglycemic first-degree relatives of patients with Type 2 diabetes. Ann Intern Med 1999 (July 6th): In press.
11. Patsch J, Miesenböck G, Hopferwieser T, et al. Relation of triglyceride metabolism and coronary artery disease. Studies in the postprandial state. Arterioscler Thromb 1992;12:1336-45.
13. Axelsen M, Eliasson B, Joheim E, Arvidsson Lenner R, Taskinen M-R, Smith U. Lipid intolerance in smokers. J Internal Med 1995;237:449-455.
17. Malmström R, Packard C, Caslake M, et al. Defective regulation of triglyceride metabolism by insulin in the liver in NIDDM. Diabetologia 1997;40:454-62.
21. The DCCT Research Group. Epidemiology of severe hypoglycemia in the diabetes control and complications trial. Am J Med. 1991;90:450-9.
27. Axelsen M, Wesslau C, Arvidsson Lenner R, Lönnroth P, Smith U. Bedtime uncooked cornstarch supplement prevents nocturnal hypoglycaemia in intensively treated IDDM subjects. J Internal Med 1999;245:229-36.
30. Axelsen M, Lenner RA, Lönnroth P, Smith U. Breakfast glycemic response in patients with type 2 diabetes: Effects of bedtime dietary carbohydrates. Eur J Clin Nutr 1999: In press. 41. Axelsen M, Lönnroth P, Arvidsson Lenner R, Smith U. Suppression of the nocturnal free fatty acid levels by bedtime cornstarch in NIDDM. Eur J Clin Invest 1997;27:157-63.
42. Axelsen M. Nocturnal and postprandial metabolism in diabetes mellitus. With special reference to lipid intolerance and the second-meal effect . Göteborg: Göteborg University, 1999.
[Innehåll] [Redaktören] [Ordföranden] [Sett & Hört] [Aktuell Info] [Redaktionen]
[Arkivet] [Länkar] [Diskussionsforum] [Diabetes Update]
