
Gå tillbaka
Diabetes makulaödem 2012 – en gigantisk utmaning
Helle Kalm, överläkare
S:t Eriks Ögonsjukhus, Stockholm.
Ett paradigmskifte har ägt rum när det gäller behandling av diabetiskt makulaödem. Från att rädda och bevara syn talar man nu om att förbättra och återställa syn. Från laserbehandling med termisk destruktion av synceller till nu farmakologisk behandling med läkemedel som sprutas in i ögats glaskropp. Men nya behandlingen med intravitreal injektion ställer skärpta krav på diagnostik, gränsöverskridande samarbete och patientcompliance, samtidigt som den utmanar resursfördelningen inom sjukvården. Frågan är om även sjukvårdsprocessen behöver ett paradigmskifte.
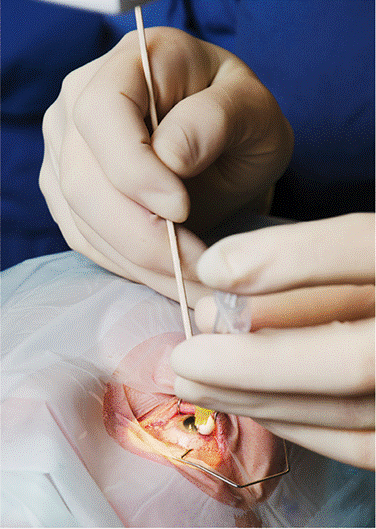
Bild 1: Intra-vitreal injektion. Foto: Eva Tov. S:t Eriks Ögonsjukhus
Mekanismer för diabetes makulaödem
Näthinnans kärl innehåller två typer av celler, pericyter (kontraktilitet) och endothelceller (tillväxt). Vid för högt blodsocker dör pericyterna, kärlstabiliteten påverkas och blodflödet ändras. Resultatet blir syrebrist i näthinnan och ämnet VEGF (Vascular Endothelial Growth Factor) blir mätbart i ögat (1); angiogenetiska processen aktiveras.
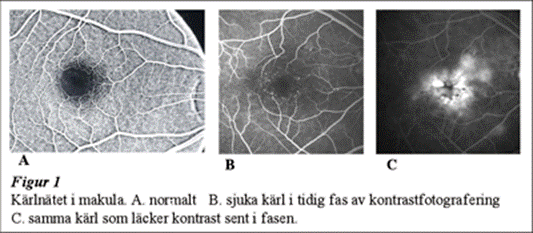
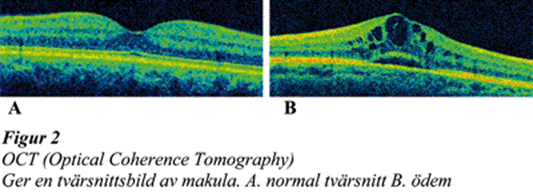
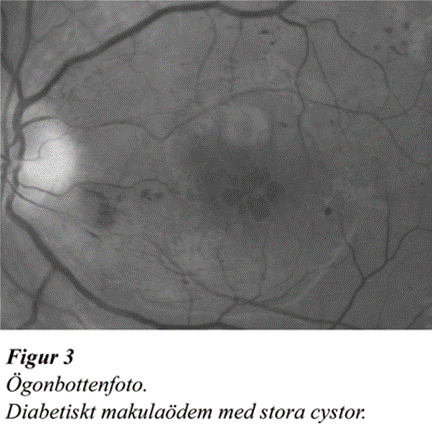
VEGF stimulerar endotelcellernas tillväxt vilket leder till kärlnybildning, proliferativ diabetes retinopati och förstör ocludin och claudin som binder ihop endothelcellerna i kärlväggens tight-junctions (2). Därvid uppstår läckage genom kärlväggen. Läckage i kärl-nätet runt gula fläcken (makula), ger makulaödem, Figur 1 a,b,c och synskärpan försämras irreversibelt utan behandling. Tjockleken av makulaödemet kan mätas med OCT (Optical Coherence Tomography, Figur 2 a,b. Vid uttalat makulaödem ses ofta cystor i centrum, figur 3.
Terapeutiska angreppspunkter är att öka syresättningen lokalt,
t ex med laser (3) eller att blockera VEGF med anti-VEGF.
Patogenesen vid diabetiskt makulaödem är dock mera komplicerat än så. Förutom VEGF tillkommer en inflammatorisk komponent. Årets bästa och prisbelönta oftalmologiska avhandling skriven av Carin Gustavsson (4), behandlar ämnet. Bristande anti-VEGF respons på diabetiskt makulaödem illustreras också snyggt i ett annat arbete där just inflammatoriska mediatorer som inte svarar på specifik anti-VEGF behandling identifieras (5). Kortison har således också en funktion i behandlingen.
Inflammation efter katarakt – operation - förstör resultatet
En inflammatorisk reaktion efter speciell katarakt (grå starr) operation ger också ödem. Om den inflammatoriska reaktionen pålagras en redan existerande inflammation kan resultat långsamt försämras och synen ett antal veckor efter operationen bli sämre än innan.
Patienter med svårare grader av diabetesretinopati löper högre risk att råka ut för detta. Risken för postoperativ svullnad i gula fläcken är speciellt stor vid befintligt makulaödem, även tidigare laserbehandlad torr sådan samt vid proliferativ diabetesretinopati (6). Ögondropparnanepafenac, Nevanac® i kombination med rimexolon, Vexol® har nyligen rekommenderats som effektiv behandling (7). Ett speciellt omhändertagande av riskpatienter inför kataraktoperation är viktig för att uppnå bästa synprognosen.
Dagens behandlingsarsenal - och kommande läkemedel
Laserbehandlingen är fortfarande state of the art behandling vid proliferativ diabetesretinopati. Ökade syremängd nedgraderar VEGF och kärlkonstriktionen till följd av ökat syre gör att de nybildade kärlen vissnar bort. Primär användning av anti-VEGF utan förberedande laserbehandling kan däremot leda till näthinneavlossning vid proliferativ diabetes retinopati. Makulaödem som ej går in centralt (i fovea) d v s extrafovealt ödem kan också framgångsrikt behandlas med laser enbart. Ny typ av laser, multispotlasern, är effektivare och mindre smärtsam än single-spot (8).
Fovealt makulaödem, däremot, behandlas med ranibizumab, Lucentis®, en monoklonal antikropp, som sedan mars 2011 är godkänd för ändamålet eller med bevacizumab, Avastin® ett off-label ”systerpreparat” välanvänt för behandling av metastaserande coloncancer, se DiabetologNytt 2010 årg 23 nr 6. Båda har en effekttid på ca 4-6 veckor. Om anti-VEGF inte ger effekt finns dexametason, Ozurdex® som för tillfället testas vid diabetiskt makulaödem (9) och som redan godkänts för behandling av makulaödem vid oftalmologiska, venösa ocklusioner (10). Ozurdex® är en steroid som inbäddat i en liten stav injiceras i ögats glaskropp för att därefter över månader avge aktiva substansen innan den löses upp. Effekttiden är vid venösa ocklusioner i ögat 4-6 månader.
Läkemedelskostnaden för Lucentis® är ca 9.000 SEK och för Avastin® ca 300 SEK efter fraktionering av den i cancervården använda standardampullen. Prisskillnaden har medfört att vissa landsting i Sverige och vissa länder i Europa valt Avastin® med hänvisning till CATT – studien (11) där signifikanta skillnader i behandlingseffekt och risk-events inte kunde påvisas mellan de två preparaten. CATT – studien är utfört av NIH och täcker 1–års uppföljning av Lucentis® respektive Avastin® behandlade patienter med våt åldersdegeneration i makula i USA.
Kommande preparat är VEGF Trap-Eye (12) en ny monoklonal antikropp som förväntas bli introducerad i Europa våren 2012. Effekttiden är 2 månader till skillnad från Lucentis® ca 1 månad och antal besök kan därmed reduceras något. Fluocinolon acetonid, Illuvien® (13) än så länge godkänd enbart i USA är en synnerligen potent steroid med effekt på ödem som stått upp till 3 år men med obligatorisk katarakt och hög risk för steroidglaukom som oönskade bieffekter. Effektiden är 30 månader.
Injektionsbehandling – en resurskrävande utmaning
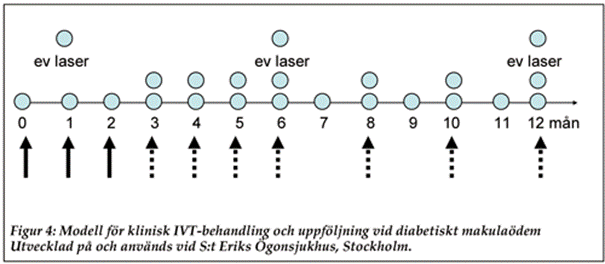
Restore studien (14) som ligger till grund för behandling med Lucentis® är välbeskiven i tidigare i DiabetologNytt, se ovan. Figur 4 visar en modell för reducerad, klinisk behandling och uppföljning utvecklad vid St: Eriks Ögonsjukhus, Stockholm. Värd intresset är att totala antalet besök som omfattar synprövning, mätning av ödemtjocklek med OCT, skopi av ögonbotten, laserbehandling och injektioner uppgår allt som allt till 23 vid maximal behandling. Härtill kommer sprutkostnader som tidigare nämnts. Behandlingen är alltså kostsam och resurskrävande.
Styrkan i framtidens läkemedel ligger därför inte bara i effekten utan också i effekttiden av läkemedlet (längre intervall mellan behandlingarna) och därmed lägre personalkostnader och lägre sjukfrånvaro bland patienterna.
Patientcompliance – en förutsättning för behandling
Patientens förmåga och motivation är en förutsättning för att genomföra den besöksfrekventa behandlingen som kan ta upp till 1 år eller mera. Hur klarar den äldre, trötta, sjukliga patienten alla besök? Etiska konflikter kan också uppstå i situationer där patienter med utländsk bakgrund eller utlandsbosatta pensionärer enbart vistas sporadiskt i Sverige.
Optimal behandling –är gränsöverskridande
God diabetesvård ger bästa synprognosen vilket tydligt framgår av de basala, viktiga medicinska interventionsstudierna: DCCT för typ 1 (15), EDIC med bonus paketet ”metabolt minne” (16) samt UKPDS för typ 2 diabetes (17). God metabol kontroll, normal lipidprofil och välreglerat blodtryck kan inte ersättas av nålstick i ögat. Gemensamma ansträngningar med samarbete över specialistgränserna förblir värdefullt.
Diabetesögonvården –
i behov av förvandling?
Diabetesögonvården är i och med injektionsbehandlingen resurskrävande och komplicerad eftersom den genererar många olika besök och ur många synpunkter är multidisciplinär. Härtill kommer att det rör sig om kroniska patienter. Injektionsterapi används även för andra vanliga typer av makulaödem inom oftalmologin och diabetespatienterna tävlar därför om uppmärksamheten. För 30 år sen tillkom screening som lösning på dåtidens problem. Nu saknas steg 2 för differentierad uppföljning och individualiserad behandling. Min personliga reflektion är att diabetesögonvården snarast behöver nya, intelligenta journalapplikationer som underlättar diagnostik, automatiserar rapportering, information och kommunikation, validerar data och kvalitetssäkrar värden.
Slutsats
Diabetiskt makulaödem kan nu behandlas framgångsrikt med läkemedel som sprutas in i ögats glaskropp, intra-vitreal injektionsbehandling. Synen kan i bästa fall förbättras och återställas mot tidigare endast att kunna bevaras. Dagens terapiarsenal omfattar anti-VEGF och i en framtid steroidpreparat men lasern är fortfarande aktuell som komplement. Injektionsbehandling mångfaldigar besöksfrekvensen vilket medför skenande personalkostnader. God diabetesvård är bästa prevention men garanterar inte immunitet. Vårdprocessen för diabetesretinopati behöver sannolikt ett akut nytänkande för att klara resursproblemen – ytterligare ett paradigmskifte?
Referenser:
1. . Aiello LP, Avery RL, Arrigg PG, Keyt BA, Jampel HD, Shah ST, Pasquale LR, Thieme H, Iwamoto MA, Park JE, et al. Vascular endothelial growth factor in ocular fluid of patients with diabetic retinopathy and other retinal disorders. N Engl J Med. 1994 Dec 1;331(22):1480-7.
2. . Kvanta A. Ocular angiogenesis: the role of growth factors. Acta Ophthalmol Scand. 2006 Jun;84(3):282-8. Review.
3. . Stefánsson E. The therapeutic effects of retinal laser treatment and vitrectomy. A theory based on oxygen and vascular physiology. Acta Ophthalmol Scand. 2001 Oct;79(5):435-40.
4. . Carin Gustavsson: Inflammatory Mediators in Diabetic Retinopathy. Avhandling. ISBN 978-91-86443-15-3.
5... Funk M, Schmidinger G, Maar N, Bolz M, Benesch T, Zlabinger GJ, Schmidt-Erfurth UM. Angiogenic and inflammatory markers in the intraocular fluid of eyes with diabetic macular edema and influence of therapy with bevacizumab. Retina. 2010 Oct;30(9):1412-9.
6. . Kim SJ, Equi R, Bressler NM. Analysis of macular edema after cataract surgery in patients with diabetes using optical coherence tomography. Ophthalmology. 2007 May;114(5):881-9.
7... Warren KA, Bahrani H, Fox JE. NSAIDs in combination therapy for the treatment of chronic pseudophakic cystoid macular edema. Retina. 2010 Feb;30(2):260-6.
8... Diabetic Retinopathy Clinical Research Network, Brucker AJ, Qin H, Antoszyk AN, Beck RW, Bressler NM, Browning DJ, Elman MJ, Glassman AR, Gross JG, Kollman C, Wells JA 3rd. Observational study of the development of diabetic macular edema following panretinal (scatter) photocoagulation given in 1 or 4 sittings. Arch Ophthalmol. 2009 Feb;127(2):132-40.
9... Herrero-Vanrell R, Cardillo JA, Kuppermann BD. Clinical applications of the sustained-release dexamethasone implant for treatment of macular edema. Clin Ophthalmol. 2011;5:139-46.
10. Haller JA, Bandello F, Belfort R Jr, Blumenkranz MS, Gillies M, Heier J, Loewenstein A, Yoon YH, Jacques ML, Jiao J, Li XY, Whitcup SM; OZURDEX GENEVA Study Group. Randomized, sham-controlled trial of dexamethasone Intravitreal implant in patients with macular edema due to retinal vein occlusion. Ophthalmology. 2010 Jun;117(6):1134-1146.
11. CATT Research Group, Martin DF, Maguire MG, Ying GS, Grunwald JE, Fine SL, Jaffe GJ. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. N Engl J Med. 2011 May 19;364(20):1897-908
12. Do DV, Schmidt-Erfurth U, Gonzalez VH, Gordon CM, Tolentino M, Berliner AJ, Vitti R, Rückert R, Sandbrink R, Stein D, Yang K, Beckmann K, Heier JS. The DA VINCI Study: phase 2 primary results of VEGF Trap-Eye in patients with diabetic macular edema. Ophthalmology. 2011 Sep;118(9):1819-26.
13. Pearson PA, Comstock TL, Ip M, Callanan D, Morse LS, Ashton P, Levy B, Mann ES, Eliott D. Fluocinolone acetonide intravitreal implant for diabetic macular edema: a 3-year multicenter, randomized, controlled clinical trial.
..... Ophthalmology. 2011.
Aug;118(8):1580-7.
14. Diabetic Retinopathy Clinical Research Network, Elman MJ, Aiello LP, Beck RW, Bressler NM, Bressler SB, Edwards AR, Ferris FL 3rd, Friedman SM, Glassman AR, Miller KM, Scott IU, Stockdale CR, Sun JK. Randomized trial evaluating ranibizumab plus prompt or deferred laser or triamcinolone plus prompt laser for diabetic macular edema. Ophthalmology. 2010 Jun;117(6):1064-1077.
15. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. The Diabetes Control and Complications Trial Research Group. N Engl J Med. 1993 Sep 30;329(14):977-86.
16. White NH, Sun W, Cleary PA, Danis RP, Davis MD, Hainsworth DP, Hubbard LD, Lachin JM, Nathan DM. Prolonged effect of intensive therapy on the risk of retinopathy complications in patients with type 1 diabetes mellitus: 10 years after the Diabetes Control and Complications Trial. Arch Ophthalmol. 2008 Dec;126(12):1707-15.
17. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study (UKPDS) Group. Lancet. 1998 Sep 12;352(9131):837-53. Erratum in: Lancet 1999 Aug 14;354(9178):602.
|Upp|
