
Gå tillbaka
HbA1c i fokus
Jan-Olof Jeppsson, Marcus Österbrand och Gunnar Nordin
Inledning
HbA1c är den viktigaste analysen för att följa metabol
kontroll vid behandling av diabetes mellitus. HbA1c utgör den fraktion
av hemoglobin, till vilken glukos bundits under blodkroppens levnad, som
är ca 120 dagar, och är samtidigt en indikator på liknande
inbindning av glukos till 100-tals andra plasma- och membranproteiner.
Ju fler perioder med hyperglykemi, desto högre HbA1c-värden.
Vid insatt intensivbehandling sjunker HbA1c snabbast under de första
8 veckorna och därefter mera långsamt under ytterligare 8 veckor
(1 ). Hemolytisk anemi med förkortad överlevnad av blodkroppar
ger falskt låga HbA1c-värden. Av samma bilogiska skäl
uppvisar patienter med hemoglobinopatier som t.ex. sickelcellshemoglobin,
HbAS samt HbAC och HbAE för låga HbA1c-värden i förhållande
till medelplasmaglukoskoncentrationen. Uremi eller stora intag av salicylat
kan ge falskt höga värden med några av HbA1c metoderna.
Glykerat hemoglobin har varit ett samlingsbegrepp för hemoglobinmolekyler
med glukos bundet till olika bindningsställen. Numera definieras
HbA1c mera exakt som den andel av hemoglobinets betakedjor som har glukos
bundet till den första aminosyran valin. Det fullständiga och
systematiska kemiska namnet för denna nya mätstorhet är:
"Hb(betakedja)-Deoxyfruktosylhemoglobin (betakedja); substansfraktion".(2)
Det gamla namnet "HbA1c" kommer dock att leva kvar i dagligt
tal, och användas på remisser och i laboratorierapporter.
Vid Diabetsforum i Linköping 1995 etablerades konsensus inom profession och Svenska Diabetesförbundet i vilken det fastslogs att den svenska Mono S metoden skulle införas som "nationell jämförelsemetod" i Sverige (3). Vid denna tid valde också Japan sin egen HbA1c-metod som nationell jämförelsemetod. Varken DCCT metoden eller någon av de nämnda HbA1c-metoderna uppfyller krav på att vara internationell referensmetod (4). En referensmetod ska vara garanterat stabil över lång tid, oberoende av vem som utför mätningarna, och ska mäta det sanna värdet med minimal osäkerhet.
Hur relaterar HbA1c till diabeteskomplikationer?
Genom att sänka sitt medel-HbA1c med 10% från t.ex. 7% till
6,3% minskas patientens risk för nytillkomna ögonskador med
nästan 50% (5). Vi förstår därmed också att
minskningar från t.ex 7% till 6,6%, d.v.s. med 0,4 procentenheter,
också är av klinisk betydelse för den enskilde patienten
och av betydelse att kunna urskilja med dagens laboratoriemetoder. Det
finns ett exponentiellt samband mellan HbA1c och risker för diabeteskomplikationer
(5, 6). Detta innebär t.ex. att när HbA1c ökar från
7% till 8% så ökar riskerna betydligt mer än när
det ökar från 6% till 7%. Detta är av stor betydelse för
såväl patienten som ur ett nationellt diabetesperspektiv.
För den enskilde individen innebär det att höga HbA1c-värden
ger mycket stora risker, men också att eventuella sänkningar
från dessa nivåer ger stora vinster. T.ex. reduceras den framtida
risken för ögonskador för en patient nästan lika mycket
genom att sänka medel-HbA1c från 10% till 9% som en minskning
från 9% till 5%. Det är viktigt att patienter med dålig
metabol kontroll får denna information och inspireras av kunskapen
om att varje liten förbättring innebär stora vinster. En
förbättring från 10% till 8,5% kan i många fall
göra att de allvarligaste diabeteskomplikationerna uteblir. Vi bör
dock vara medvetna om att det inte finns någon tröskel, d.v.s.
ingen nivå under vilken riskerna är 0 (7). Vinster görs
även från 6% till 5% och t.o.m. har patienter i normalpopulationen
betydligt högre risk för död vid t.ex. HbA1c 4,5% än
3,5% (5-8).
Om alla diabetespatienter i Sverige skulle ha HbA1c 5% istället för
6%, skulle det förmodas bli ca 2100 färre patienter som får
nya ögonskador per år (figur 1). Lägger vi därtill
att liknande starka riskgradienter finns mellan HbA1c och njurkomplikationer,
bensår, amputationer och att riskerna även ökar för
stroke, hjärtinfarkt och död blir betydelsen än mer påtaglig
(9).
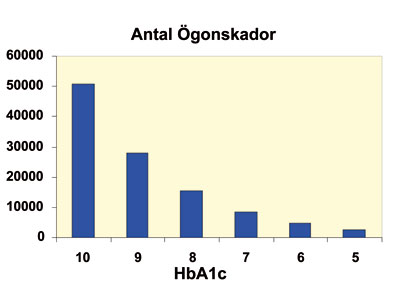
Figur 1: Beräknat antal patienter i Sverige med nya
ögonskador per år om alla diabetespatienter skulle ha en viss
HbA1c-nivå. Beräkningar gjorda utifrån approximation
att det finns 400.000 diabetespatienter i Sverige och resultat från
DCCT-studien avseende nytillkomna ögonskador / 100 patientår
och HbA1c-nivå (5).
Utöver att HbA1c:s relationer till diabeteskomplikationer är
exponentiell och att små förändringar har betydelse så
har aktuella HbA1c-värden också relation till diabeteskomplikationer
som uppkommer långt fram i tiden. Vi skulle kunna kalla det ett
metabolt minne. Ett sådant minne har tidigare visats för ögon-
och njurskador (10, 11) men nyligen också för hjärtkärlsjukdom
och död (12).
I denna nyliga uppföljning av DCCT-studien visades att patienter
löper mycket större risk för hjärtkärlsjukdom
i framtiden om de tidigare legat högt i HbA1c. För de individer
i DCCT, d.v.s. typ 1 diabetespat-
ienter i ca 30-årsåldern, som hade HbA1c 6% jämfört
med 8% i 6,5 års tid blev det ca 60% färre som fick en hjärtinfarkt,
stroke eller död under de påföljande 11 åren, även
om HbA1c då var detsamma. (figur 2) Detta innebär att HbA1c
måste förbättras så tidigt som möjligt i sjukdomen.
Det är också viktigt att patienten får information om
att värdena har betydelse in i framtiden och att det inte är
säkert att diabeteskomplikationer stannar upp när HbA1c förbättras.
Det finns annars en risk att våra diabetespatienter tror att det
räcker att börja förbättra HbA1c, när ett fotsår
uppstår eller en ögonförändring uppträder.
Sammanfattningsvis har små förändringar av HbA1c betydelse,
de största vinsterna görs på de högsta nivåerna
och värdena har betydelse i framtiden.
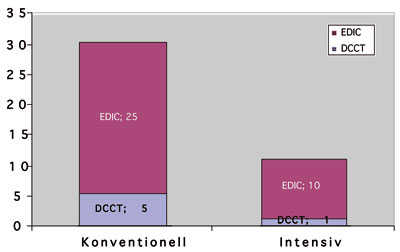
Figur 2: Antal hjärtinfarkt, stroke eller cardiovaskulär
död under DCCT respektive under de 11 påföljande åren
(EDIC). Under DCCT som pågick i genomsnitt under 6,5 års tid
var HbA1c med svenska mått ca 6% i intensivgruppen och 8% i konventionellgruppen.
Under de påföljande 11 åren var HbA1c i princip samma,
ca 7%, för de båda grupperna. Ändå uppstod det signifikant
fler macrovaskulära skador i den tidigare konventionellbehandlade
gruppen. Figur framtagen från data från såväl DCCT
som EDIC (12, 13).
Kvalitet i den svenska diabetesvården
Nationella Diabetesregistret (NDR) jämför HbA1c-nivåer
för olika vårdenheter och subgrupper av patienter. T.ex. jämförs
i NDR hur stor andel av typ1 diabetespatienterna, som uppfyller målen
vid olika medicinkliniker. Skillnaderna är ibland stora. Diab-Base
är ett kvalitetsutvecklingssystem som används vid ett 20-tal
sjukhus i landet och i Norge (14). Med hjälp av detta kan man studera
HbA1c-nivåer för vilka subgrupper man vill och för hur
lång tid tillbaka som helst sedan systemets introduktion på
den enskilda kliniken.
År 2003 jämfördes HbA1c-nivåer för flera olika
subgrupper av patienter vid olika sjukhus. För vissa sjukhus kunde
man se att HbA1c för alla subgrupper skilde sig gentemot HbA1c-nivån
för motsvarande subgrupper på andra sjukhus (figur 3). Det
var då mest sannolikt att förmoda att fel på laboratoriemetoden
måste föreligga, då det inte var rimligt att tro att
mer eller mindre exakt lika patienter skulle skilja sig så kraftigt
som 0,6 procentenheter i HbA1c. Det kunde också konfirmeras att
det fanns sjukhus som låg så mycket som 0,6 procentenheter
fel i den egna HbA1c metoden. Alla systematiska fel större än
0,1 procentenheter för laboratoriemetoden påverkar populationsjämförelser.
Det är viktigt att vara medveten om att deltaga i EQUALIS kvalitetssäkringsprogram
eller att vara ackrediterad av SWEDAC är inte synonymt med att den
egna HbA1c metoden är välfungerande. Det krävs således
att den enskilda vårdenheten agerar om EQUALIS mål inte uppfylls.
För ett välfungerande och jämförbart NDR är välfungerande
laboratoriemetoder av stor vikt.
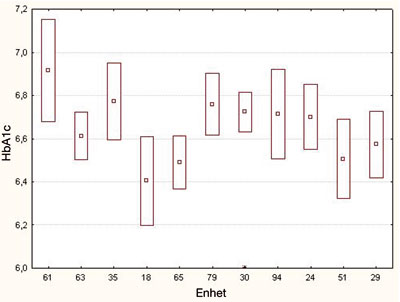
Figur 3: Bilden visar medel-HbA1c och standard error of
the mean för en selekterad patientgrupp (4-dosregim,insulindos <0,5
E/kg) vid 11 olika sjukhus. För två sjukhus avvek medel-HbA1c
konsekvent även när andra subgrupper jämfördes. Detta
indikerade sannolikt problem i den egna labmetoden vilket senare kunde
bekräftas. Kontroll av den egna laboratoriemetoden är av stor
vikt för den enskilde patienten och för att resultat i NDR ska
vara jämförbara. Tack till Journalia AB och Diab-Base användare.
Internationell standardisering
Den använda HbA1c metoden för DCCT- och UKPDS-studierna bestämmer
också komponenter som inte tillhör HbA1c-fraktionen. Trots
detta är den fortfarande "standardmetod" i stora delar
av världen på grund av kopplingen till den mycket viktiga information
som kommit fram vid olika kliniska studier. I Sverige har vi haft tillgång
till Mono S metoden, utvecklad i samarbete med dåvarande Pharmacia
Fine Chemicals i Uppsala, en metod som är mera specifik (15).
International Federation Clinical Chemistry and Laboratory Medicine (IFCC),
som är en paraplyorganisation för alla nationella föreningar
för klinisk kemi i världen, startade 1995 utveckling av en referensmetod
för HbA1c. Principen för referensmetoden är följande:
Hemoglobin molekylen spjälkas i flera peptider med enzymet endoproteinas,
Glu-C och de terminala heaxapeptiderna (de första sex aminosyrorna
i betakedjan) med och utan glukos kvantiteras efter separation med HPLC
kombinerad med masspektrometri eller kapillärelektrofores. Kvoten
mellan dessa peptider med och utan glukos uttrycks som % eller mmol HbA1c/mol
Hb. Systemet kalibreras med blandningar av renframställt HbA1c och
HbA0 i olika proportioner. Metoden godkändes 2002 och ett nätverk
av internationellt certifierade laboratorier bestämmer nu det "sanna
HbA1c värdet" för provmaterial två ggr per år
(16). Dessa material användes därefter för att få
riktighet hos HbA1c reagenser från ett 30-tal olika tillverkare.
Tills vidare konverterar företagen därefter resultaten till
DCCT-, japansk- eller Mono S nivå för att varje land tills
vidare ska kunna behålla sin nuvarande nationella standard. IFCC's
specifika referensmetod ger 1,3 -1,9% enheter lägre värden än
DCCT och 0,6-0.9% enheter lägre än Mono S. IFCC-metoden är
idag internationellt accepterad som ankare och referensmetod, men den
kliniska implementeringen dröjer. Tanken är att alla HbA1c-resultat
ska vara likvärdiga över hela världen Det finns flera anledningar
till att en global övergång till IFCC- standardisering fördröjts.
Om IFCC resultaten fortfarande skulle anges som %HbA1c har man pekat på
riskerna att de något lägre siffrorna skulle kunna misstolkas
av patienterna som en klinisk förbättring (17). Under en övergångsperiod
skulle det dessutom vara förvirrande att särskilja flera olika
sorters HbA1c-resultat. Därför finns en rekommendation från
IFCC att byta måttenheten '% HbA1c' till 'mmol/mol', d.v.s. mmol
glykerade hemoglobinkedjor per mol hemoglobinkedjor. I praktiken kan man
säga att det är som att ange koncentrationen som '‰ HbA1c'.
Det numeriska värdet blir således 10 gånger större;
"6,0% HbA1c" med Mono S systemet kommer att motsvaras av "5,2
% HbA1c" med IFCC-systemet, eller uttryckt med den nya föreslagna
måttenheten, av "52 mmol/mol". I tabell 1 illustreras
sambandet mellan Mono S- DCCT- och IFCC-nivåer. I det kliniskt intressanta
området är DCCT-nivåerna ca 1 procentenhet högre
än Mono S.
Det har även rått oenighet i namnfrågan. Om analysen
någon gång ska byta namn, så vore ett bra tillfälle
i samband med övergången till IFCC-standardisering. Termen
'HbA1c' har varit svår att etablera i några delar av världen,
där man associerar förledet 'Hb...' till en hematologisk sjukdom.
I USA används därför ofta termen 'A1C'. I Europa vill dock
de flesta länder behålla 'HbA1c', som är väl inarbetat
i diabetesvården.
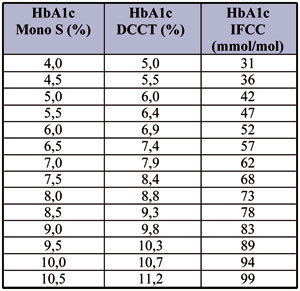
Tabell 1 för omvandling mellan tre
"olika HbA1c"
Ekvation för förhållandet mellan
HbA1c IFCC och HbA1c Mono S:
(a) HbA1c, IFCC (mmol/mol) = 10,45 x HbA1c, Mono S (%) - 10,62
Ekvation för förhållandet mellan
HbA1c DCCT och HbA1c Mono S:
(b) HbA1c, DCCT (%) = 0,956 x
HbA1c, Mono S (%) + 1,18
Sambandet (a) mellan Mono S och IFCC's referensmetod baseras på aktuella jämförelser mellan metoderna, och skiljer sig därför en aning från det samband som publicerats tidigare. Sambandet (b) mellan DCCT och Mono S baseras på (a) tillsammans med publicerat samband mellan DCCT och referensmetoden (4).
Samband mellan HbA1c och medelplasmaglukos
Det finns ett välkänt samband mellan HbA1c och medelplasmaglukos
(MPG) från ett flertal olika studier (18-21).Vissa centra i USA
redovisar HbA1c tillsammans med MPG med en konverteringsekvation. Det
skulle kunna ha pedagogiska fördelar för den enskilde patienten
att också rapportera MPG. Det är av stor vikt vid en eventuell
övergång till att rapportera medelplasmaglukos tillsammans
med HbA1c, att korrelationen är mycket stark. Det finns annars en
risk, att om HbA1c översätts till ett felaktigt värde för
medelplasmaglukos för vissa patienter, så görs terapibyten
på felaktiga grunder med påföljd att t.ex. risker för
hypoglykemier uppstår och felaktig riskprediktion sker.
Tre internationella organisationer ( IDF, ADA och EASD) har därför
initierat en ny studie vid 11 olika centra och över 4 olika kontinenter,
där patienter med typ1 och typ 2 diabetes samt icke diabetiker ingår.
Syftet är att fastställa sambandet mellan HbA1c och MPG med
moderna och kontrollerade metoder för olika diabetestyper, genetik
och etnicitet. I bakgrunden finns fortfarande den helt specifika IFCC-metoden
för HbA1c. Målet är att undersöka om ett HbA1c-resultat
kan räknas om och besvaras som MPG, vilket är ett starkt önskemål
från ledande medlemmar i de aktuella organisationerna. Kompromissen
kan vara att svara både med HbA1c och HbA1c konverterat till MPG
med en global ekvation. Under den pågående utredningens gång
rekommenderas att alla länder behåller sina nationella system
i väntan på någon form av gemensam global övergång.
MPG resultaten kommer att presenteras på EASD-kongressen i Amsterdam
i september, men därefter kommer säkert flera överläggningar
och tolkningar av dessa resultat göras, innan konklusioner kan dras
och eventuella åtgärder ske.
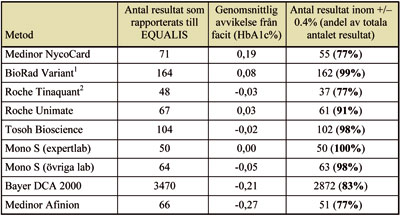
1) Omfattar instrumenten Variant, Variant II and D-10.
2) Omfattar även TinaQuant-reagens på andra instrument än
Roches instrument Hitachi och Modular.
Tabell 2. HbA1c-resultat för EQUALIS provmaterial under 2006
Nationell kvalitetsövervakning
Mätinstrumentets riktighet är viktig, oavsett om analysen sker
vid det centrala laboratoriet eller den lokala mottagningen. Alla laboratorieanalyser
har ett visst slumpfel och en genomsnittlig avvikelse (bias) jämfört
med ett sant värde. För att få veta hur stora dessa fel
är för just det använda instrumentet, måste laboratoriet/mottagningen
delta i ett externa provningsjämförelser. Ett sådant kan
vara lokalt eller nationellt organiserat, och innebär att man regelbundet
mäter HbA1c i ett prov med okänd HbA1c nivå.
Efter mätning får man veta det "sanna värdet"
och resultaten bearbetas statistiskt. Vid konsensusmötet 1995 (3)
kom man överens om att laboratoriets dag-till-dag variation (dvs
mellanliggande precision) bör vara <3% uttryckt som variationskoefficient
(CV), eller motsvarande 0,2%-enheter på nivån HbA1c = 6,5%.
Den tillåtna spridningen mellan olika laboratorier beslutades också
1995 till att vara maximalt 3% CV.
Sedan 2002 har EQUALIS förtydligat och konkretiserat kvalitetsmålen
för att gör dessa enklare att förstå. Enligt dessa
bör avvikelsen för det enskilda resultatet från det sanna
värdet vara maximalt +/- 0,4 HbA1c %-enheter, inklusive osäkerheten
i det sanna värdet. Det senare uppskattas till +/- 0,1 HbA1c-procentenheter.
Tyvärr finns det fortfarande metoder och laboratorier, som inte uppfyller
dessa krav, men flera metoder visar på en klar och lovande förbättring
efter introduktion av certifierade kalibratorer hos reagenstillverkarna.(tabell
2)
Det bästa sättet att försäkra sig om laboratoriets
aktuella kvalitet är att granska de grafiska månadsrapporterna
från EQUALIS, som finns tillgängliga på alla laboratorier.
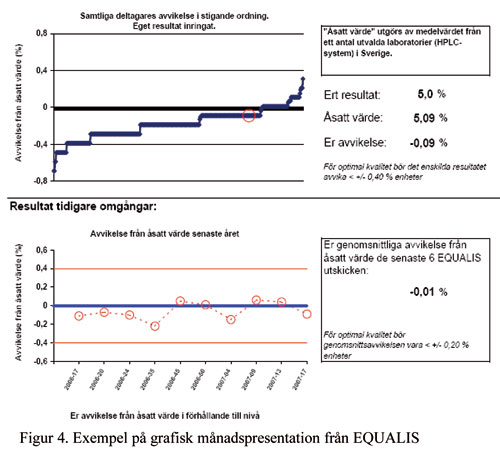
Ett exempel på en sådan rapport finns i figur 4. Det övre
diagrammet visar de samlade resultaten från det aktuella utskicket
rangordnat från lägsta till högsta rapporterade värde
i Sverige, med det egna resultatet inringat. Det nedre diagrammet visar
det egna laboratoriets konsekutiva resultat ett år tillbaka i tiden.
Den genomsnittliga avvikelsen från det sanna värdet under en
6 månaders period bör vara högst +/- 0,2% enheter HbA1c.
Bra analyskvalitet i HbA1c testen är en förutsättning för
att de behandlingsmål som används i kliniken skall bli meningsfulla
och för att patientresultaten ska vara jämförbara i de
nationella diabetesregistren.
Referenser
1.Tamara Y, Shima K. Kinetics of HbA1c, Glycated Albumin, Fructosamine
and Analysis of Their Weight Functions Against Preceding Plasma Glucose
Level. Diabetes Care 1995;18:440-7.
2.Nordin G, Dybkaer R on behalf of the IFCC-IUPAC C-NPU. Recommendation for Term and Measurement Unit for 'HbA1c'. Clin Chem Lab Med 2007 (accepted for publication).
3.Arnqvist H, Wallensteen M, Jeppsson JO. Standard spikad för långtidsmått på blodsocker. Läkartidningen 1997;50:4789-90.
4.Hoelzel W, Weykamp C, Jeppsson JO, Miedema K et al IFCC reference system for measurement of hemoglobin A1c in human blood and the national standardization schemes in the United States, Japan, and Sweden: a method-comparison study. Clin Chem 2004;50:166-74.
5.DCCT Study Group (1995) The relationship of glycemic exposure (HbA1c) to the risk of development and progression of retinopathy in the diabetes control and complications trial Diabetes Aug;44(8):968-983.
6.DCCT Study Group (1993) The Effect of intensive treatment of diabetes
on the development and progression of long-term complications in insulin-dependent
diabetes mellitus N Engl J Med Sep 30;329(14):977-986.
7.DCCT Study Group (1996) The absence of a glycemic threshold for the
development of long-term complications: the perspective of the Diabetes
Control and Complications Trial. Diabetes Oct;45(10):1289-1298
8.Khaw KT, Wareham N, Luben R et al. (2001) Glycated haemoglobin,
diabetes, and mortality in men in Norfolk cohort of european prospective
investigation of cancer and nutrition (EPIC-Norfolk). BMJ. 2001 Jan 6;322(7277):15-18.
9.Stratton IM, Adler AI, Neil HA et al. (2000) Association of glycaemia
with macrovascular and microvascular complications of type 2 diabetes
(UKPDS 35): prospective observational study. BMJ Aug 12;321(7258):405-412.
10.The Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications Research Group. (2000) Retinopathy and nephropathy in patients with type 1 diabetes four years after a trial of intensive therapy. N Engl J Med Feb 10;342(6):381-389. Erratum in: N Engl J Med 2000 May 4;342(18):1376.
11.Writing Team for the Diabetes Control and Complications Trial/Epidemiology
of Diabetes Interventions and Complications Research Group. (2003) Sustained
effect of intensive treatment of type 1 diabetes mellitus on development
and progression of diabetic nephropathy: the Epidemiology of Diabetes
Interventions and Complications (EDIC) study. JAMA Oct 22;290(16):2159-2167.
12.Nathan DM, Cleary PA, Backlund JY et. al. (Diabetes Control and Complications
Trial/Epidemiology of Diabetes Interventions and Complications (DCCT/EDIC)
Study Research Group.) (2005) Intensive diabetes treatment and cardiovascular
disease in patients with type 1 diabetes. N Engl J Med Dec 22;353(25):2643-2653.
13.DCCT Study Group (1995) Effect of intensive diabetes management
on macrovascular events and risk factors in the Diabetes Control and Complications
Trial. Am J Cardiol May 1;75(14):894-903.
14.Osterbrand M, Fahlen M, Oden A, Eliasson B. A method to predict the
metabolic effects of changes in insulin treatment in subgroups of a large
population based patient cohort. Eur J Epidemiol. 2007;22(3):151-7. Epub
2007 Feb 6.
15.Jeppsson JO, Jerntorp P, Sundkvist G, Englund H, Nylund V. Measurement of Hemoglobin A1c by a New Liquid Chromatographic Assay: Methodology, Clinical Utility and Relation to Glucose Tolerance Evaluated. Clin Chem 1986;32:1867-72.
16.Jeppsson JO, Kobold U et al. Approved IFCC Reference Method for Measurement of HbA1c in Human Blood. Clin Chem Lab Med 2002;40(1):78-89.
17.Hanås R. Psychological Impact of Changing the Scale of reported
HbA1c Results Affects Metabolic Control. Diabetes Care 2002;25:2110-11.
18.Rohlfing CL, Wiedmeyer HM, Little RR, England JD, Goldstein DE. Defining
the Relationship Between Plasma Glucose and HbA1c. Diabetes Care 2002;25(2):275-78.
19.Hempe JM, Gomez R, McCarter RJ Jr, Chalew SA. High and low hemoglobin
glycation phenotypes in type 1 diabetes: a challenge for interpretation
of glycemic control. J Diabetes Complications. 2002 Sep-Oct;16(5):313-20.
20.Derr R, Garrett E, Stacy GA, Saudek CD. Is HbA(1c) affected by glycemic
instability? Diabetes Care. 2003 Oct;26(10):2728-33.
21.McCarter RJ, Hempe JM, Gomez R, Chalew SA. Biological variation in HbA1c predicts risk of retinopathy and nephropathy in type 1 diabetes. Diabetes Care. 2004 Jun;27(6):1259-64.
Jan-Olof Jeppsson, Docent
f.d. Överläkare, Klinisk Kemi, Malmö
Marcus Österbrand, ST-läkare i
diabetologi och endokrinologi,
Uddevalla Sjukhus.
Doktorand vid Diabetes Centrum
Sahlgrenska Universitetssjukhuset
Gunnar Nordin, VD, EQUALIS , Uppsala,
|Upp|
