
Gå tillbaka
DIABETESVÅRDEN BEHÖVER
HÖRAS
Felrapportering om insulinpumpar och andra hjälpmedel kommer huvudsakligen från tillverkarna. På Läkemedelsverket skulle man vilja se mer aktivitet från diabetesvårdens sida när det gäller att anmäla tillbud och följa upp händelser som inträffar med patienternas produkter. Tillverkarna och vården behöver också bli bättre på att kommunicera - i synnerhet om risker och kontraindikationer.
Intervju
med Mats Ohlsson,
Läkemedelsverket.
Av Margaretha Hellenberg,
medicinjournalist
Av 18 felrapporter till Läkemedelsverket om olyckor
eller tillbud som gällt insulinpumpar under åren 2005-2006 kom 3 från
vården. 99 rapporter om fel på glukosmätare kom alla från
tillverkaren. Det händer också att patienter hör av sig men det
hör till undantagen. Många har direktkontakt med tillverkaren, vilket
är bra anser man på verket, men vården borde vara mer aktiv när
det gäller att följa upp patienternas produkter. Ofta vet inte diabetesmottagningen
att det varit problem över huvud taget.
- Det är en tystlåten
bransch, säger Mats Ohlson, som arbetar med tillsynsfrågor vid Läkemedelsverkets
enhet för medicinsk teknik. När rapporterna bara kommer från tillverkarna
måste vi själva ta kontakt med vården. Det tar mycket tid och
stjäl resurser. Vården behöver bli bättre på att se
produkternas begränsningar, som inte alltid framgår i tillverkarnas
marknadsföring.
Mats Ohlson tycker att tillverkarna har en övertro
på hur mycket vården kan ha kontroll över. Vården å
sin sida har ibland en övertro på produkterna, att de är hundraprocentigt
säkra och inte behöver support.
Läckande pumpar
Mellan 5 000 och 6 000 av landets diabetiker har insulinpumpar. När något
hänt, till exempel läckage, påstår företagen ofta att
produkten har använts fel. Är insulinpumpar kanske alltför komplicerade?
Tar tillverkarna verkligen hänsyn till att de ska skötas av "vanligt
folk"? Mats Ohlson menar att vården måste fundera över om
och när det fungerar att lägga över kvalificerad medicinsk teknik
och infusionsterapi på patienterna själva.
Även om de flesta
patienter är duktiga med sina pumpar så är de inte tillräckligt
utbildade och man kan inte lita på larmet om pumpen går sönder
under sömnen. Han tycker inte att tillverkarna kommunicerar problemen tillräckligt
bra och vården frågar inte vid upphandlingen vilka kontraindikationer
som finns. En av tillverkarna har i sin bruksanvisning angett att pumpterapi inte
rekommenderas till människor som inte klarar av att ta fyra blodglukostester
per dag och att ha kontinuerlig kontakt med vården.
- Kanske är
det bara en tiondel av patienterna med insulinpumpar och andra hjälpmedel
som egentligen borde ha dem, undrar Mats Ohlson. Det kan vara vanskligt med hemanvändning
om den inte kombineras med support och tillsyn. Folk skickas hem med medicintekniska
produkter som ger bättre livskvalitet. De slipper vara bundna av en vårdinrättning
men i stället tummas det på säkerheten. Man får vara beredd
på att ta en del risker. Så är det med alla hjälpmedel.
Rollatorer och elrullstolar är heller inte hundraprocentigt säkra. Det
är en risk-nytta-ekvation som man måste räkna med, så man
ska kanske inte bli förvånad om det händer något.
Rutiner
och åtgärder
När en felrapport från tillverkaren
kommer till Läkemedelsverket begärs kompletterande information från
vården. Likaså följs användarrapporter upp genom att man
hämtar in kommentar från tillverkaren. Verkets handläggare kan
också göra inspektioner på plats. Varje rapport kan avse många
händelser, som exempelvis de 5 rapporter som åren 2005-2006 inkom beträffande
reservoarer och som representerade ett 50-tal händelser. Enstaka fel kan
slå igenom kraftigt i statistiken. En felaktig typ av slang kan till exempel
generera många händelser.
Tillverkaren utreder i samarbete med
användaren och söker förklaringar. Verket gör tillsammans
med tillverkare och användare en riskanalys av det enskilda fallet och av
tillverkarens ansvar. Hur farligt var det? Vad kunde ha hänt? Hur hade tillverkaren
tänkt när produkten designades? Därefter värderas problemets
omfattning, vilka åtgärder som ska vidtas och sedan följas upp.
Tillverkaren kan åläggas korrigerande åtgärder eller att
ta tillbaka produkten. Om inget annat har fungerat kan Läkemedelsverket som
en sista utväg utfärda marknadsförbud när det handlar om fara
för folkhälsan. Allt som är av vikt för ärendet registreras
i verkets diarium. Tillverkarna kan också anmodas att gå ut med förtydliganden
och kompletterande information när något inträffat, till exempel
varna för att utsätta insulinpumpen för starka magnetfält
som kan förstöra vissa komponenter i pumpen.
- Ju mer vi får
veta, desto mer kan vi göra, säger Mats Ohlson. Vi finns för patienternas
skull och får vi argument från vården att göra något
så gör vi det. Vi behöver ha tillräckligt bra information,
annars kan vi inte bedöma vidden av problemet och hur allvarligt det är.
De allt större företagen kan vara svåra att tampas med för
enskilda. Där kan vi hjälpa till genom vårt internationella nätverk.
Vi kan få stort genomslag om vi har tillräckligt "på fötterna".
När det gäller andra produkter har vi från Sverige lyckats påverka
stora företag eftersom vi haft god kontakt med användarna.
Underrapportering
Enligt Läkemedelsverket kan fel och tillbud vara fler än de som
kommer till verkets kännedom. Företagen är dock skyldiga att följa
reglerna för tillbudsrapportering. Samarbetsviljan har blivit bättre
men den varierar.
- Om vi kommer på dem med att inte ha rapporterat
vad de borde, så är det en allvarlig anmärkning. En del har vi
bra kommunikation med, medan andra gömmer sig bakom sitt godkännande
ända tills det ställs på sin spets. Ibland kan det vara segt att
få in uppföljningsrapporter, vilket betyder ökad arbetsbelastning
för oss, säger Mats Ohlson. Tillverkarna går inte vidare när
de ser att användaren knappat fel utan skjuter problemen ifrån sig.
Företagen kräver blodglukostester fyra gånger om dagen, men
inom vården vet man att det i realiteten mera handlar om en gång per
dag - om ens det. Tillverkarens idealbild stämmer inte, menar han och efterlyser
mera förståelse för den lokala användaren. Vården kan
bli bättre på att rapportera, följa upp och att läsa bruksanvisningar
och information från tillverkarna före inköp för att bättre
kunna utvärdera produktens användbarhet och begränsningar. Anledningen
till att vården rapporterar tillbud i så liten utsträckning tror
Mats Ohlson kan bero på okunskap om till exempel rapporteringsvägar,
rädsla för att dra på sig kritik från patienterna för
bristande information och inte minst det extraarbete det innebär. Sjukvården
har redan mycket som ska rapporteras och detta blir en sak till.
- Vi har
inte mandat att tala om för vården hur den ska göra - det är
Socialstyrelsens sak - men vi brukar påtala då och då att det
hade varit bra om de hade anmält. Viljan är nog god men vi ser inga
resultat. Ett önskemål från Läkemedelsverkets sida är
också bättre samarbete mellan tillverkare och användare vid anmälningsfall
för att ta tillvara material för riskvärdering. Det händer
att det som gått sönder inte sparats och det går då inte
heller att utvärdera.
Material, dvs slangar eller pumpar, som använts
när det inträffat en olycka eller ett tillbud ska skickas till tillverkaren
eller lämnas till sjukhusets medicintekniska avdelning för vidare utredning.
Patienter bör informeras om att inte kasta defekta produkter. Redan vid upphandlingen
kan vårdgivaren/landstinget fråga tillverkaren hur man ska gå
tillväga vid reklamationer, hur kontaminerat material ska hanteras, om det
ska skickas rengjort etc.
Om händelsen skulle vara föremål
för polisutredning ska man avvakta beslut från polisen om vad som ska
göras med den använda produkten. Tillverkaren ska ändå alltid
underrättas omedelbart. Rapporteringen sker även till Läkemedelsverket
men inga produkter ska skickas dit.
Socialstyrelsen håller just nu på
att uppdatera sina föreskrifter (SOSFS 2001:12) om medicintekniska produkter
med tydligare direktiv än de nuvarande om agerande vid olyckor och tillbud
där medicintekniska produkter varit inblandade. De beräknas komma ut
i höst.
Mats Ohlson på Läkemedelsverket, handläggare för tekniska problem med insulinpumpar och glukosmätare, finns på tel 018-17 46 00 och epost: Mats.Ohlson@mpa.se
Läkemedelsverket
Box 26
751 03 UPPSALA
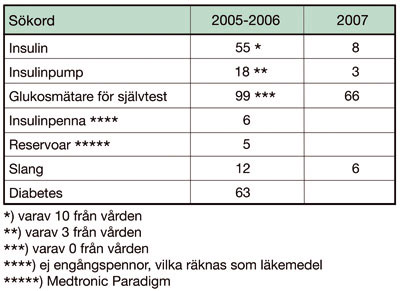
Felrapporter
om olyckor/tillbud
Diabetesprodukterna är uppdelade på flera
koder, varför Läkemedelsverkets statistik inte visar en entydig bild.
Sökning enligt nedan ger dock en ungefärlig uppfattning. Varje rapport
kan dessutom representera flera händelser.
Kommentarer
från några diabetessjuk-sköterskor och diabetologer
Det är bra att Läkemedelsverket uppmanar vården att vara mer aktiva när det gäller att anmäla tillbud och händelser med patienternas diabetesprodukter. Detta bör vara en självklarhet och vi bör alla bli bättre på detta! Det upskattas mycket att verket är positivt till ökad kommunikation med vården kring dessa frågor. Det vore bra med ett möte i höst mellan Läkemedelsverket och Svensk Förening för Diabetologi (SFD), Svensk Förening för Sjuksköterskor i Diabetesvård (SFSD) och barnläkarföreningen för att få en fortsatt dialog bl.a. kring hur man kan underlätta rapporteringsvägar, återrapportering, sammanställningar, etc. Det vore också bra med snabb kontakt från verket efter rapport om tillbud.
Vad är
det som gäller?
Socialstyrelsen har formulerat krav på att
vårdgivare skall rapportera olyckor och tillbud med medicintekniska produkter
till tillverkaren (dennes ombud) och till Läkemedelsverket. Kraven finns
inskrivna i Socialstyrelsens föreskrifter och allmänna råd (SOSFS
2001:12) om användning och egentillverkning av medicintekniska produkter
i hälso- och sjukvården. Anmälningsplikten gäller:
- de som orsakat en patients, en användares eller någon annans död,
- de som orsakat att en patient, en användare eller någon annan fått sin hälsa allvarligt försämrad, eller
- de som kunnat orsaka en patients, en användares eller någon annans död eller att en patient, en användare eller någon annan kunnat få sin hälsa allvarligt försämrad.
Osäkra på anmälningsvägarna
Att vi är dåliga på att anmäla kan bero på att vi
är osäkra på anmälningsvägarna som verket skriver. Vi
har även genom åren invaggats i tron att det räcker att en part
anmäler händelsen och litat på att företagen gjort det när
vi kommunicerat med dem. De har dock i många fall väntat med att anmäla
till verket till efter deras egen utredning är gjord och detta har inneburit
en fördröjning, ibland en avsevärd sådan.
Uppfattningen
om att professionen har en övertro på produkternas säkerhet är
överdriven. Många års erfarenhet av pumpbehandling gör att
vi är medvetna om att det kan uppkomma tekniska problem med insulinpumpbehandling
och därför har de flesta av våra mottagningar satt upp rutiner
kring hur vi hanterar fel med glukosteststickor/mätare och insulinpumpar.Professionen
tar också i sitt dokument om behandlingsriktlinjer en ställning för
en fortsatt hög utbildnings- och säkerhetsnivå.
Kliniska
riktlinjer
När det gäller insulinpumpbehandling finns nationellt
framtagna Kliniska riktlinjer för insulinpump-behandling vid diabetes hos
vuxna och barn-ungdom, senast publicerade i DiabetologNytt 2007/1. Då en
patient startar med t.ex. insulinpump övervägs noga behandlingsindikationer
och patienten genomgår därefter en omfattande träning och genomgång
av användandet som sedan följs upp kontinuerligt. Allt detta ingår
i förskrivningsansvaret som ju också finns reglerat av Socialstyrelsen.
Det vi lär våra patienter är att de skall testa sitt blodsocker
minst fyra ggr per dag vid pumpbehandling, gärna mer och att absolut krav
är att testa varje dag morgon och kväll för att upptäcka tecken
på ketoacidos.
Att pumppatienter som regel endast testar 0-1 ggr/dag
är inte vår erfarenhet.
Pumparna har många säkerhetslarm
inbyggda av olika slag men det finns inte larm för om nålen glider
ut ur "kroppen". Pumpen märker naturligtvis ingen skillnad på
om den levererar insulinet i underhusfettet eller i sängen.
Kalkylerad
risk
Det är sant som handläggaren på Läkemedelsverket
skriver att man får vara beredd på att ta en del risker.
För
många är insulinpumpsbehandling den i nuläget, bästa tillgängliga
diabetesbehandlingen och bygger på att diabetesteamet gjort ett noggrant
sammanvägande av det medicinska behovet och eventuella risker och är
inte något som lättvindigt förskrivs, utan tvärtom efter
systematiska förberedelser. Uppföljningen är sedan noggrann och
kontinuerlig i enlighet med riktlinjerna.
Fungerar inte pumpbehandlingen
av olika skäl skall den ifrågasättas och avslutas.
Längre
ner på denna sidan finner Du ett exempel på en blankett att använda
vid
avvikelsehantering.
Förslag på blankett från DiabetologNytt för avvikelsehantering

|Upp|
